感染性心内膜炎
①感染性心内膜炎のリスク因子(例:糖尿病、透析患者)をおさえる
②focus不明の発熱の鑑別として、最後まで感染性心内膜炎を検討する
③感染性心内膜炎を疑ったら、血液培養3セット採取!
Points
・菌の種類、患者の基礎疾患などにより臨床像は非常に多彩で、古くより診断の難しい疾患として知られる。
・“常にその可能性を鑑別診断に挙げること”が重要であり、不明熱の重要な鑑別診断である。
・弁膜症による心不全、弁輪膿瘍などの合併症を来した場合、早期に心臓血管外科の介入が必要な場合もある。
感染性心内膜炎(IE:Infective endocarditis)は弁膜や心内膜、大血管内膜に細菌集簇を含む疣贅(vegetation)を形成し、菌血症、血管塞栓、心障害など多彩な臨床症状を呈する全身性疾患である。
発症前に心臓病変(弁膜症、シャント疾患、心臓への人工物移植後)を有することが多いとされるが、基礎心疾患を有さない症例もある。
発熱、寒気や震戦、食思不振、倦怠感、体重減少など
※IEの合併症による症状や、非特異的な症状も多い!
発熱を伴うその他の疾患
医療面接
発熱の経過(特異的な熱型はなく、高熱や微熱がだらだら続くこともある)
既往歴(心疾患の既往、弁置換術の有無、糖尿病など)
診察
心雑音:新たに出現した逆流性心雑音が特徴である
末梢塞栓所見:例)Osler結節(指尖部の赤~紫色の有痛性皮下結節)、爪下線状出血
Janeway紅班(手掌・足底の無痛性小紅班)、
Roth斑(眼底の出血性梗塞で中心部が白色)
全身塞栓所見:例)脾梗塞、腎梗塞による側背部痛、
腸間膜動脈塞栓による腹痛、
脳梗塞(中大脳動脈領域や多発性脳梗塞)
IEのリスク因子
・糖尿病
・透析患者
・AIDS患者
・薬物常用者
・抜歯
・口腔内不衛生
・蜂窩織炎
・アトピー性皮膚炎
・心疾患(例:僧帽弁逸脱症)
・心疾患術後
血液検査:CBC、生化、凝固、血液ガス(敗血症やDICの合併の有無も確認)
血液培養:抗菌薬投与前に血培3セット
※抗菌薬投与後だと血培陽性率が95%から35〜40%まで低下する!
心エコー:弁尖や壁心内膜に付着した疣贅、弁周囲膿瘍、
弁の破壊所見(弁瘤や弁穿孔、新規の弁逆流)の有無を確認
その他:頭部MRI、胸腹部単純・造影CT(脳塞栓、全身性塞栓症の有無を評価)
血液培養と経食道心エコー
血液培養からグラム陽性球菌が検出されIEを疑う場合、後からでも3セット目を採取する。経胸壁心エコーのIEの検出感度は60%程度だが、経食道心エコーは感度76〜100%、特異度94〜100%と非常に診断精度が高い。
ただし、病初期には疣贅が小さく陰性と判断しかねる場合もあるため、臨床経過よりIEを疑うなら7〜10日後に再検することも検討される。
①抗菌薬(抗菌薬の選択は上級医と相談して決定する)
例)自己弁の初期治療:ABPC/SBT 3g×4/day + CTRX 2g×1/day(MRSAの可能性が低い場合)
VCM 1g(15mg/kg)×2/day + GM 1mg/kg×3/day(PCアレルギーの場合)
人工弁の初期治療:VCM 1g(15mg/kg)×2/day + GM 1mg/kg×3/day
※培養結果に応じて、de-escalationすること!
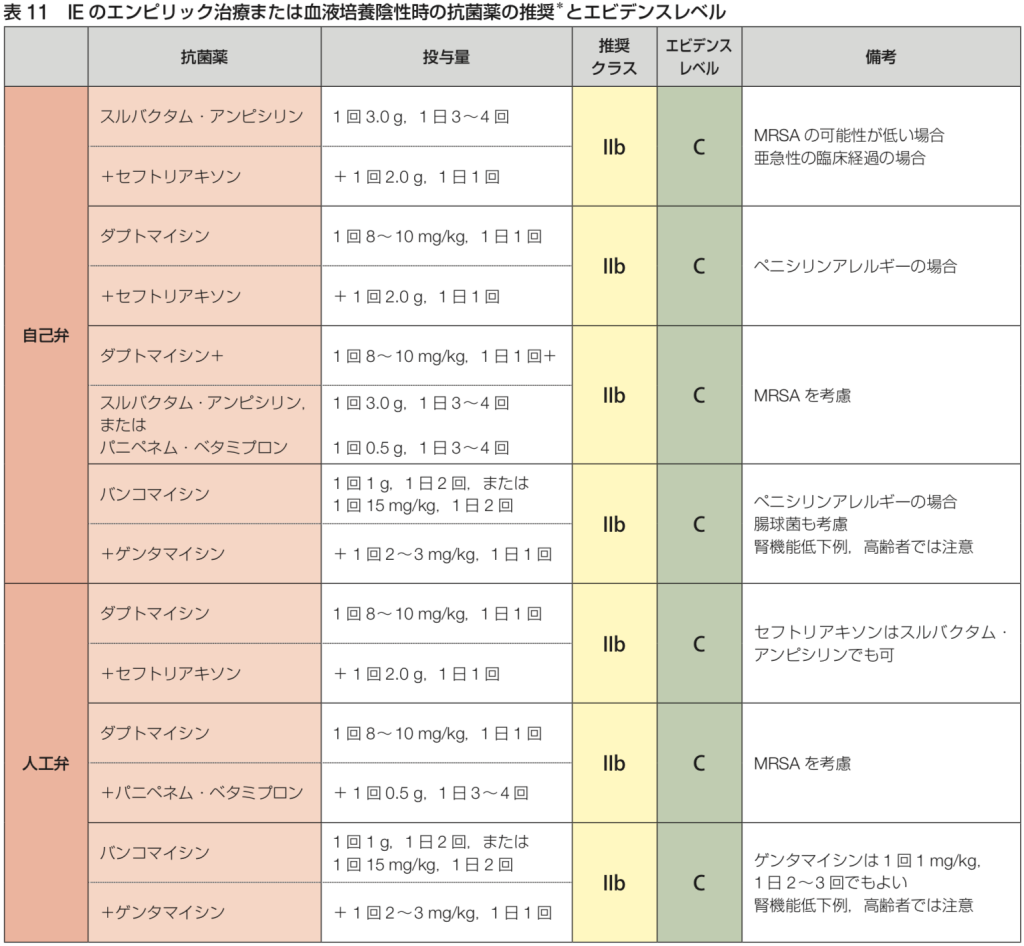
抗菌薬の初期治療
感染性心内膜炎ガイドライン(2017年改訂版)に記載されている抗菌薬の初期治療は以下の通り。
感染症に興味のある循環器内科医として、個人的な考えを少しだけ。笑
個人的には自己弁の場合、CTRX 2g×1/day+GM 60mg(1mg/kg)×3/dayで良いと思っています。
(腸球菌カバーはできていませんが、頻度は低く、後から抗生剤を変更しても遅くないと思います。)
またDAPの位置付けが非常に高いですが、基本的にはVCMからスタートで良いと思います。
それとPCGの用量はMIC<0.12であれば、1200〜1800万単位/dayまで下げて良いと思います。
TDM解析
ゲンタマイシン・バンコマイシンは入院後にTDM解析を行う必要があります。
・ゲンタマイシン:トラフ値 <1μg/mL、ピーク値 3〜5μg/mL
・バンコマイシン:トラフ値 15〜20μg/mL(初回は10〜15μg/mLでも可)
②手術
適切に手術適応の有無を判断し、心臓血管外科にコンサルトを行う。
例:IEによる弁破壊に伴う心不全症例
抗菌薬でコントロール不良なIE
人工弁に伴うIE
③合併症の治療
脳塞栓症や全身塞栓症を合併していれば、その治療も行う。
IEの主な起因菌
S.aureus(26.6%)
Oral streptococci(18.7%)
Non-oral streptococci(17.5%)
Enterociccu(10.5%)、CNS(9.7%)
※IEの83%はグラム陽性球菌!
(Lancet 2016; 387: 882-893)
原則入院。
血液培養陰性例や培養に時間のかかる細菌もあるため一度疑ったら何度もフォローすること。
MICとMRSA菌血症/連鎖球菌性感染性心内膜炎/腸球菌性感染性心内膜炎
【MIC】
以下の3つの状況下では培養結果のMICの数値にも気を払う。
MICの値で第1選択薬のチョイスや投与期間に影響する!
①MRSA菌血症(VCM) ②連鎖球菌性感染性心内膜炎(PCG) ③肺炎球菌性髄膜炎(PCG、CTRX)【MRSA菌血症】
VCM耐性(MIC>2μg/mL)の場合、DAP(キュビシン® )を使用。
ただしDAPは肺胞サーファクタントにより賦活化するため、MRSA肺炎でVCM使用できなければLZDを考慮。
→第一選択薬は常にVCM、第二選択薬は肺以外はDAP、肺はLZD!
・DAPは皮膚・軟部組織・血液への移行性が良い。
・VCM耐性の場合、DAP耐性になっていることも多いため、しっかり高用量で治療する!
・LZDは2週間以上の投与で血小板減少が必発!【連鎖球菌性感染性心内膜炎】
PCのMICの値により治療法が変わる。
①MIC<0.12(感受性+)
・PCG 2400万単位/day(4週間) ※PCGはKが含有されており高Kに注意!
・ABPC 3g×4/day(4週間) ※CKD・高齢者・DM患者で高Kのリスクがある場合に選択
・CTRX 2g×1/day(4週間) ※透析患者・Ccr<10の場合
②MIC>0.25(感受性-)
・PCG 2400万単位/day(4週間) + GM 1mg×3/day(2週間)
・ABPC 3g×4/day(4週間) + GM 1mg×3/day(2週間)
・VCM 1g×2/day(4週間) ※PCアレルギーの場合
③MIC>1.0
感染症科にコンサルト必要(GM併用期間など)【腸球菌性感染性心内膜炎】
検査:高濃度GMでの感受性試験が必要
基準:GM MIC>500μg/mL、SM MIC>2000μg/mLで耐性と判断→相乗効果での併用効果なし
(GMが耐性だった場合にはSMも代替候補になり得る)
治療:GM MIC<500μg/mL、SM MIC<2000μg/mLであれば、アミノグリコシド系を併用して治療すべし
補足:PC系耐性の場合(特にE.faecium)の場合、VCM・DAPで治療
細胞壁合成阻害薬以外の抗菌薬(例:DAP)では、アミノグリコシド系の併用不要【腎機能障害】
PCGやABPCを大量に投与すると、腎機能障害(間質性腎炎)を認める場合がある。
腎機能低下傾向を認めたら、CTRXに変更し間質性腎炎のマーカー(β2MG・NAD・尿中好酸球など)を確認する。
GM併用時の場合、腎機能障害がPC系かGMのどちらが原因か知ることができる。